অ্যাসাইনমেন্ট : সেল ও ব্যাটারির পরিচিতি ।
শিখনফল/বিষয়বস্তু :
- সেল
- ব্যাটারি
- সেলের শ্রেণীবিভাগ
নির্দেশনা (সংকেত/ ধাপ/ পরিধি):
- সেলের ধারনা বর্ণনা করতে হবে
- ব্যাটারি ধারনা বর্ণনা করতে হবে
- সেলের শ্রেণীবিভাগ করতে হবে
উত্তর সমূহ:
এসাইনমেন্ট সম্পর্কে যে কোন প্রশ্ন আপনার মতামত জানাতে পারেন আমাদের কে YouTube : Like Page ইমেল : assignment@banglanewsexpress.com
সেলের ধারনা বর্ণনা করতে হবে
যে যন্ত্রের সাহায্যে রাসায়নিক শক্তিকে বিদ্যুৎ শক্তিতে রুপান্তর করা যায় তাকে সেল বলে।
ইলেকট্রিক সেল এমন একটি ডিভাইস যা ইলেকট্রিসিটি জেনারেট করার জন্য ব্যবহার করা হয়। এটা এমন একটি একক ইউনিট যা রাসায়নিক শক্তিকে বৈদ্যুতিক শক্তিতে রূপান্তর করে ডিসি ভোল্টেজ উৎপাদন করতে পারে।
প্রতিটি সেলে দুটি টার্মিনাল থাকে, একটি পজেটিভ এবং অপরটি নেগেটিভ টার্মিনাল। পজেটিভ টার্মিনালে লম্বা রেখা এবং নেগেটিভ টার্মিনালে ছোট রেখা দ্বারা বুঝানো হয়। নিচে চিত্র দেওয়া হলোঃ

একটি কক্ষ রাসায়নিক প্রক্রিয়ার মাধ্যমে বিদ্যুত উৎপাদন করে । অনেক ধরনের ইলেকট্রোকেমিক্যাল কোষগুলি বিদ্যুৰ্শক্তির কোষ , ইলেক্ট্রোলাইটিক কোষ , জ্বালানী কোষ এবং প্রবাহ কোষ হিসাবে থাকে । একটি কোষ একটি হ্রাস এবং অক্সিডাইসিং এজেন্টের সমন্বয় , যা শারীরিকভাবে একে অপরের থেকে পৃথক হয় ।
সাধারণত আলাদা একটি লবণ সেতু দ্বারা করা হয় । যদিও তারা শারীরিকভাবে পৃথক হয়ে থাকে তবে উভয় অর্ধেক কোষ একে অপরের সাথে রাসায়নিক যােগাযােগে থাকে ।
ইলেক্ট্রোলাইটিক এবং গ্যাসভাইক্লিক কোষ দুটি ধরনের ইলেট্রোক্রেমিক কক্ষ । উভয় ইলেক্ট্রোলাইটিক এবং গ্যাসভাইক্লিক কোষে , অক্সিডেসন – হ্রাস প্রতিক্রিয়া সঞ্চালিত হয় ।
অতএব , মূলত , একটি ইলেট্রোকেমিক্যাল সেলের মধ্যে দুটি ইলেকট্রড থাকে যা বলা হয় anode এবং একটি ক্যাথােড । উভয় ইলেকট্রোড বহিরাগত একটি উচ্চ প্রতিরােধী ভােল্টমিটার সঙ্গে সংযুক্ত করা হয় ; অতএব , বর্তমান ইলেকট্রোড মধ্যে প্রেরণ করা হবে না।এই ভােল্টমিটার অক্সিডেসন প্রতিক্রিয়া সঞ্চালিত হয় যেখানে ইলেক্ট্রোড মধ্যে একটি নির্দিষ্ট ভােল্টেজ বজায় রাখতে সাহায্য করে । অক্সিডেসন প্রতিক্রিয়াটি অ্যানডিতে সঞ্চালিত হয় , এবং হ্রাস প্রতিক্রিয়া ক্যাথােড এ সঞ্চালিত হয় । ইলেক্ট্রোড পৃথক ইলেক্ট্রোলাইট সমাধান মধ্যে নিমজ্জিত হয় ।
সাধারণত , এই সমাধানগুলি ইলেক্ট্রোডের প্রকারের সাথে সম্পর্কিত আইওনিক সমাধান । উদাহরণস্বরূপ , তামার ইলেকট্রোডগুলি তামা সলফেট সমাধানে নিমজ্জিত হয় এবং রূপালী ইলেকট্রড সিলভার ক্লোরাইডের সমাধানে নিমজ্জিত হয় । এই সমাধানগুলি ভিন্ন ; অতএব , তাদের পৃথক করা উচিত তাদের পৃথক করার সবচেয়ে সাধারণ উপায় একটি লবণ সেতু । একটি ইলেট্রোকেমিক্যাল সেল ইন , সেল সম্ভাব্য শক্তি একটি বৈদ্যুতিক বর্তমান রূপান্তরিত হয় ।
[ বি:দ্র: নমুনা উত্তর দাতা: রাকিব হোসেন সজল ©সর্বস্বত্ব সংরক্ষিত (বাংলা নিউজ এক্সপ্রেস)]
ব্যাটারি ধারনা বর্ণনা করতে হবে
ব্যাটারিঃ বৈদ্যুতিক সার্কিটে কারেন্টের পরিমাণ কমানো/বাড়ানোর জন্য বা ভোল্টেজ পরিবর্তনের জন্য কতগুলো বৈদ্যুতিক সেলকে একত্রে সংযোগ করা হয়। এই একত্রিত সেল্গুলোকে ব্যাটারি বলে।
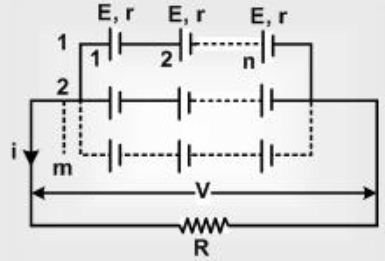
- এটি একাদিক সেলের সমন্বয়ে গঠিত।
- এর কার্যকরী রেজিস্ট্যান্সের মান বাহ্যিক বৈদ্যুতিক সংযোগের সাহায্যে কম-বেশি করা যায়।
- চাহিদামত ভোল্টেজের মান কমানো-বাড়ানো যায়।
ভােল্টেজ বা কারেন্টের পরিমাণ বা উভয়ই বৃদ্ধির জন্য প্রয়ােজনীয় সংখ্যক সেলের সংযােগ করে ব্যাটারি তৈরি করা হয় । ভােল্টেজ বৃদ্ধি করতে সেলের সিরিজ সংযােগ ,
কারেন্ট বৃদ্ধিতে প্যারালাল সংযােগ এবং ভােল্টেজ ও কারেন্টের বৃদ্ধিতে মিশ্র সংযােগ করা হয । সংযুক্ত সেলের পরিমাণ চাহিদার উপর নির্ভর করে
[ বি:দ্র: নমুনা উত্তর দাতা: রাকিব হোসেন সজল ©সর্বস্বত্ব সংরক্ষিত (বাংলা নিউজ এক্সপ্রেস)]
সেলের শ্রেণীবিভাগ করতে হবে
( ক ) প্রাইমারি সেল : যে সেল বা বিদ্যুৎ কোষ এর শক্তি একবার শেষ হলে চার্জ করে পুনরায় ব্যবহার করা যায় , তাকে প্রাইমারি সেল বা মুখ্য কোষ বলে । লেকল্যান্স সেল , ড্যানিয়েল সেল এবং ড্রাই সেল ইত্যাদি প্রাইমারি সেলের শ্রেণিভুক্ত । বর্তমানে এ ধরনের সেলের ব্যবহার সীমিত ।
প্রাইমারি সেলে রাসায়নিক পদার্থগুলাের ক্রিয়া বন্ধ হয়ে গেলে বিদ্যুৎ প্রবাহ বন্ধ হয় । তখন সে সেল আর ব্যবহার করা যায় না । এ ধরণের সেল ক্যালকুলেটর , ঘড়ি , টর্চলাইট ইত্যাদিতে ব্যবহৃত হয় । এ ধরনের সেল হতে একই রকম ভােল্টেজে বিদ্যুৎ সরবরাহ পাওয়া যায় না । ব্যবহারের ফলে ক্ষমতা শেষ হওয়ার আসেই ভােল্টেজ কিছুটা কমে যায় ।
( খ ) সেকেন্ডারি সেল : যে সেল বা বিদ্যুৎ কোষ এর শক্তি একবার শেষ হলে তা পুনরায় চার্জ করে ব্যবহার করা যায় , তাকে সেকেন্ডারি সেল বলে । ইহাকে সঞ্চয়ী বিদ্যুৎ কোষও বলা হয় । চার্জের দ্বারা বিদ্যুৎ শক্তি রাসায়নিক শক্তিতে এবং ব্যবহারের সময় রাসায়নিক শক্তি , বিদ্যুৎ শক্তিতে রূপান্তরিত হয় । ব্যবহারের ফলে চার্জ শেষ হলে আবার চার্জ করে উক্ত সেল আবার ব্যবহার করা যায় । যে রাসায়নিক বিক্রিয়ার ফলে তড়িৎ শক্তির উদ্ভব হয় সেই রাসায়নিক শক্তি সেলের মধ্যে সঞ্চিত থাকে বলে এর নামকরণ হয়েছে সঞ্চয়ী সেল ।
লিড এসিড সেল , অ্যালকালি সেল ইত্যাদি সেকেন্ডারি সেলের শ্রেণিভুক্ত । বর্তমানে সেকেন্ডারি সেল ব্যাপকভাবে ব্যবহৃত হচ্ছে । মােটর গাড়ি চালু করতে , সাবস্টেশনের নিয়ন্ত্রণ কাজে রেলের সিগন্যালে , টেলিফোন একচেঞ্জে , যানবাহন চালনা ইত্যাদি ক্ষেত্রে ইহা ব্যবহৃত হয় ।এ ধরনের সেকেন্ডারি সেল হতে প্রায় একই রকম ভােল্টজ এ বিদ্যুৎ সরবরাহ পাওয়া যায় ।
[ বি:দ্র: নমুনা উত্তর দাতা: রাকিব হোসেন সজল কপিরাইট: (বাংলা নিউজ এক্সপ্রেস)]
এসাইনমেন্ট সম্পর্কে যে কোন প্রশ্ন আপনার মতামত জানাতে পারেন আমাদের কে YouTube : Like Page ইমেল : assignment@banglanewsexpress.com
- ২০২১ সালের SSC পরীক্ষার্থীদের অ্যাসাইনমেন্ট উত্তর লিংক
- ২০২১ সালের HSC পরীক্ষার্থীদের অ্যাসাইনমেন্ট উত্তর লিংক
- ২০২১ সালের ৯ম/১০ শ্রেণি ভোকেশনাল পরীক্ষার্থীদের অ্যাসাইনমেন্ট উত্তর লিংক
- ২০২১ সালের HSC (বিএম-ভোকে- ডিপ্লোমা-ইন-কমার্স) ১১শ ও ১২শ শ্রেণির অ্যাসাইনমেন্ট উত্তর লিংক
- ২০২২ সালের ১০ম শ্রেণীর পরীক্ষার্থীদের SSC ও দাখিল এসাইনমেন্ট উত্তর লিংক
- ২০২২ সালের ১১ম -১২ম শ্রেণীর পরীক্ষার্থীদের HSC ও Alim এসাইনমেন্ট উত্তর লিংক
- ৬ষ্ঠ শ্রেণীর এ্যাসাইনমেন্ট উত্তর ২০২১ লিংক
- ৭ম শ্রেণীর এ্যাসাইনমেন্ট উত্তর ২০২১ লিংক
- ৮ম শ্রেণীর এ্যাসাইনমেন্ট উত্তর ২০২১ লিংক
- ৯ম শ্রেণীর এ্যাসাইনমেন্ট উত্তর ২০২১ লিংক
এখানে সকল প্রকাশ শিক্ষা বিষয় তথ্য ও সাজেশন পেতে আমাদের সাথে থাকুন ।







